Atomer och sånt
Kul att du fick för dig att kika in här för att se om det finns några outforskade områden i den ganska grundläggande kemin. Du kommer snart att märka att vi gör vårt bästa för att få det så roligt som möjligt.
Atomer är små. Väldigt små. Definitionen på vad som är litet kan ju förstås skilja sig, vissa tycker att en ko är ganska liten och andra tycker att saker först börjar bli små då de blir i storlek som en tändsticka. Oavsett hur du väljer att definiera litet kan jag dock garantera att du tycker att atomer är ganska små (för de är onekligen mindre än både en tändsticka och en ko). Faktum är, att både tändstickan, kon, datorn framför dig, du själv och allt annat runtomkring dig består av atomer.
Atom är grekiska och betyder odelbar, vilket man på senare tid kommit fram till att den inte alls är (men de kom på ordet ett ganska bra tag innan de märkte att den faktiskt gick att dela och när de upptäckte det kändes det väl lite sent att ändra). Atomen har en kärna, tänk på en äppelkärna ungefär, fast extremt mycket mindre (då även äppelkärnan precis som allt annat består av atomer). I kärnan finns protoner och neutroner, vilket du kan läsa om nedan. Runt om denna kärna finns elektroner, som kretsar omkring i en otroligt hög hastighet. Det atomen består allra mest av är faktiskt vakuum, och eftersom allt består av atomer så betyder det att allting överallt till allra största delen består av vakuum (alltså består allting till största delen av ingenting, vilket ju är en lite underhållande tanke, eller skrämmande, det beror på hur man väljer att se på saken). Atomens vikt består i princip bara av atomkärnan.
Nedan ser du en modell av en heliumatom.
Källor:
http://sv.wikipedia.org/wiki/Atom
http://www.human-academy.com/vetenskaper/naturvetenskap/grundlaggande_kemi.asp
Atom är grekiska och betyder odelbar, vilket man på senare tid kommit fram till att den inte alls är (men de kom på ordet ett ganska bra tag innan de märkte att den faktiskt gick att dela och när de upptäckte det kändes det väl lite sent att ändra). Atomen har en kärna, tänk på en äppelkärna ungefär, fast extremt mycket mindre (då även äppelkärnan precis som allt annat består av atomer). I kärnan finns protoner och neutroner, vilket du kan läsa om nedan. Runt om denna kärna finns elektroner, som kretsar omkring i en otroligt hög hastighet. Det atomen består allra mest av är faktiskt vakuum, och eftersom allt består av atomer så betyder det att allting överallt till allra största delen består av vakuum (alltså består allting till största delen av ingenting, vilket ju är en lite underhållande tanke, eller skrämmande, det beror på hur man väljer att se på saken). Atomens vikt består i princip bara av atomkärnan.
Nedan ser du en modell av en heliumatom.
Källor:
http://sv.wikipedia.org/wiki/Atom
http://www.human-academy.com/vetenskaper/naturvetenskap/grundlaggande_kemi.asp
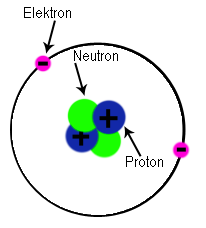
Elektroner är väldigt små. En proton (se längre ner på sidan) väger ungefär 1836 gånger mer, och en proton i sig är ju väldigt liten. Elektronerna är negativt laddade ("minusladdade") far runt atomkärnan i en väldig fart. Du kanske tycker att grannens nya bil går fort? Den är ingenting i jämförelse med en elektron (även om grannens nya bil kanske ändå kan kännas mer imponerande för somliga, märkligt).
Antalet elektroner i en atom är lika många som antalet protoner i kärnan (Om du har fem saker med "plusladdning" måste du också ha 5 saker med "minusladdning" för att det allt som allt inte ska bli någon laddning). Är elektronerna fler eller färre än antalet protoner blir atomen en jon och har då en laddning. Är det fler elektroner än protoner blir jonen negativ, är det färre elektroner blir den positiv.
Källor:
http://www.human-academy.com/vetenskaper/naturvetenskap/grundlaggande_kemi.asp
http://sv.wikipedia.org/wiki/Elektron
Antalet elektroner i en atom är lika många som antalet protoner i kärnan (Om du har fem saker med "plusladdning" måste du också ha 5 saker med "minusladdning" för att det allt som allt inte ska bli någon laddning). Är elektronerna fler eller färre än antalet protoner blir atomen en jon och har då en laddning. Är det fler elektroner än protoner blir jonen negativ, är det färre elektroner blir den positiv.
Källor:
http://www.human-academy.com/vetenskaper/naturvetenskap/grundlaggande_kemi.asp
http://sv.wikipedia.org/wiki/Elektron
Precis som majoriteten av sakerna på denna sida är neutroner små. De är dock större än elektroner och något större än protoner. Tillsammans med protoner bildar neutroner atomernas kärna. Neutronerna har ingen laddning men verkar inte särskilt ledsna för det (får medge att jag aldrig frågat någon neutron, men jag har aldrig heller hört dem klaga).
Nu kan man ju börja tjura över att de där neutronerna bara är i kärnan och tar plats när de inte ens är laddade, men viss funktion har de faktiskt. Protonerna har positiv laddning och om du någon gång testat att hålla två lika delar av magneter emot varandra, så har du märkt att dessa stöter ifrån varandra. Alla protoner har samma laddning. Neutronerna finns alltså där lite för att medla fred mellan protonerna i kärnan, som annars inte alls är så sugna på att vara ihop med varandra. Samma typ av grundämne kan ha olika många neutroner i kärnan. Olika antal neutroner i kärnan ger olika isotoper av ämnet (mer om isotoper finns att läsa under "Är du lite mer kemist?").
Källor:
http://sv.wikipedia.org/wiki/Neutron
Nu kan man ju börja tjura över att de där neutronerna bara är i kärnan och tar plats när de inte ens är laddade, men viss funktion har de faktiskt. Protonerna har positiv laddning och om du någon gång testat att hålla två lika delar av magneter emot varandra, så har du märkt att dessa stöter ifrån varandra. Alla protoner har samma laddning. Neutronerna finns alltså där lite för att medla fred mellan protonerna i kärnan, som annars inte alls är så sugna på att vara ihop med varandra. Samma typ av grundämne kan ha olika många neutroner i kärnan. Olika antal neutroner i kärnan ger olika isotoper av ämnet (mer om isotoper finns att läsa under "Är du lite mer kemist?").
Källor:
http://sv.wikipedia.org/wiki/Neutron
Förutom neutroner finns också små trevliga (eller otrevliga, jag har faktiskt aldrig umgåtts med dem i någon större utsträckning) protoner i atomens kärna. Protonerna är positivt laddade, de har alltså "plusladdning". Även dessa är små (förvånande, inte sant?), dock väger de mer än neutroner och elektroner. Trots detta väger de väldigt lite, en proton väger ungefär 0,0000000000000000000000000016726 kg (eller 1,6726·10^-27 kg om det känns bättre). Jämför med ett mjölkpaket som väger 1 kg (protoner är visserligen enligt min mening en aning mer spännande än mjölk, men det beror förmodligen på vem man frågar).
Antalet protoner i atomkärnan bestämmer vilket grundämne det är. Det blir alltså lite som protonernas identitetskort och visar vilken atom de är. Är det en proton i kärnan är grundämnet väte, är det 16 så är det svavel osv.
Källor
http://sv.wikipedia.org/wiki/Proton
Antalet protoner i atomkärnan bestämmer vilket grundämne det är. Det blir alltså lite som protonernas identitetskort och visar vilken atom de är. Är det en proton i kärnan är grundämnet väte, är det 16 så är det svavel osv.
Källor
http://sv.wikipedia.org/wiki/Proton
Nu tänker ni "Va? har elektronerna skal?" och börjar fundera över vem som lyckas med den imponerande bedriften att skala dem. Så är inte riktigt fallet. Med elektronskal menas att man mer eller mindre tänker sig att elektronerna befinner sig i skal (så är inte riktigt fallet egentligen, men förenklat så).
Det innersta elektronskalet kan som max innehålla 2 elektroner (och känns på så sätt lite udda med så pass få, men det verkar inte så deprimerad över det). Resterande kan innehålla fler. Innersta skalet heter K, nästa L, därefter M osv. Det yttersta skalet har aldrig mer än 8 elektroner, även om skalet i sig om det inte är det yttersta egentligen kan innehålla fler (oktettregeln).
Hur elektronskalen fylls på är ganska begripligt och trevligt i början åtminstone, sedan blir det lite mer rörigt. Men om man radar upp de första 18 ämnena i periodiska systemet får man en ganska överskådlig bild på hur det fungerar till en början åtminstone. Understrukna siffror innebär att det är valenselektroner, vad valenselektron innebär kan du läsa om längre ner på sidan.
Ämne Antal i K Antal i L Antal i M Atomnummer
Väte (H) 1 1
Helium (He) 2 2
Litium (Li) 2 1 3
Beryllium (Be) 2 2 4
Bor (B) 2 3 5
Kol (C) 2 4 6
Kväve (N) 2 5 7
Syre (O) 2 6 8
Fluor (F) 2 7 9
Neon (Ne) 2 8 10
Natrium (Na) 2 8 1 11
Magnesium (Mg) 2 8 2 12
Aluminium (Al) 2 8 3 13
Kisel (Si) 2 8 4 14
Fosfor (P) 2 8 5 15
Svavel (S) 2 8 6 16
Klor (Cl) 2 8 7 17
Argon (Ar) 2 8 8 18
Nedan ser du en bild med fördelningen av elektroner i elektronskalen för ämnet Argon som är en ädelgas med atomnummer 18. För att förtydliga vilket skal elektronerna ligger i har de i samma skal samma färg.
Källor:
http://www.chem4free.info/kemiskolan/kemikurs/document/konfig.htm
http://www.naturvetenskap.org/hogstadiekemi/atomer/elektroner
http://sv.wikipedia.org/wiki/Elektronkonfiguration
Det innersta elektronskalet kan som max innehålla 2 elektroner (och känns på så sätt lite udda med så pass få, men det verkar inte så deprimerad över det). Resterande kan innehålla fler. Innersta skalet heter K, nästa L, därefter M osv. Det yttersta skalet har aldrig mer än 8 elektroner, även om skalet i sig om det inte är det yttersta egentligen kan innehålla fler (oktettregeln).
Hur elektronskalen fylls på är ganska begripligt och trevligt i början åtminstone, sedan blir det lite mer rörigt. Men om man radar upp de första 18 ämnena i periodiska systemet får man en ganska överskådlig bild på hur det fungerar till en början åtminstone. Understrukna siffror innebär att det är valenselektroner, vad valenselektron innebär kan du läsa om längre ner på sidan.
Ämne Antal i K Antal i L Antal i M Atomnummer
Väte (H) 1 1
Helium (He) 2 2
Litium (Li) 2 1 3
Beryllium (Be) 2 2 4
Bor (B) 2 3 5
Kol (C) 2 4 6
Kväve (N) 2 5 7
Syre (O) 2 6 8
Fluor (F) 2 7 9
Neon (Ne) 2 8 10
Natrium (Na) 2 8 1 11
Magnesium (Mg) 2 8 2 12
Aluminium (Al) 2 8 3 13
Kisel (Si) 2 8 4 14
Fosfor (P) 2 8 5 15
Svavel (S) 2 8 6 16
Klor (Cl) 2 8 7 17
Argon (Ar) 2 8 8 18
Nedan ser du en bild med fördelningen av elektroner i elektronskalen för ämnet Argon som är en ädelgas med atomnummer 18. För att förtydliga vilket skal elektronerna ligger i har de i samma skal samma färg.
Källor:
http://www.chem4free.info/kemiskolan/kemikurs/document/konfig.htm
http://www.naturvetenskap.org/hogstadiekemi/atomer/elektroner
http://sv.wikipedia.org/wiki/Elektronkonfiguration
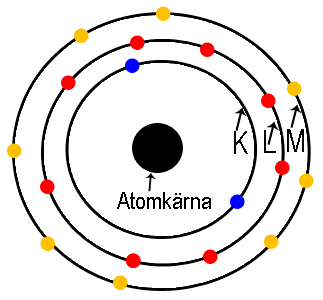
Nu har vi tittat på vad elektronskal är, och lärt oss att det inte är ett hölje runt elektronerna. De elektroner som finns i det yttersta elektronskalet kallas för valenselektroner. Hur många valenselektroner ett ämne har betyder en hel del för hur ämnet beter sig. När vi pratar om beteende i det här fallet pratar vi i huvudsak om hur reaktiva de är och liknande, inte huruvida de har bra bordsskick, är sociala eller äter morötter på ett ovanligt trevligt sätt då detta inte riktigt är aktuellt i fråga om atomer.
Har atomerna 8 valenselektroner alternativt 2 om det är i K-skalet så är det yttersta skalet fullt. Det kan då inte få plats fler valenselektroner. Atomer som har fullt med valenselektroner är väldigt nöjda och glada och inte alls sugna på att reagera med andra ämnen. De atomer som är nöjda, glada och stabila redan utan att behöva göra något för att bli det kallas ädelgaser, dessa kan du läsa mer om längre ner på sidan.
Valenselektroner är som sagt de elektroner som befinner sig allra längst bort ifrån kärnan, vilket också innebär att det är dem som påverkas av minst kraft ifrån kärnan. Detta i sin tur gör att de kan reagera med andra ämnen och ge ifrån sig elektroner, eller få fler elektroner som andra ämnen gett bort. Till skillnad från oss människor som kanske inte riktigt resonerar som så att "Okej, jag har bara en cykel, då ger jag bort den!" så fungerar det lite så att ju färre valenselektroner ett ämne har, desto mer sugen är det på att ge bort dem. En detalj som kan tilläggas är väl att det inte riktigt fungerar som så att om du har en cykel och ger bort den, så kan du plötsligt ha 8 cyklar istället. Så kan det dock fungera för atomer (de har ju visserligen gett bort en elektron, och har då en elektron mindre allt som allt, men i det här fallet är cyklarna alltså valenselektroner, inte elektroner). Ger natrium bort den enda elektronen som den har i sitt yttersta skal (se tabellen ovan) så har den plötsligt 8 valenselektroner och då fullt i det yttersta skalet och känner sig genast gladare. Atomer som har fler eller färre elektroner än antalet protoner i kärnan kallas för joner. Mer om joner kan du läsa längre ner.
Källor:
http://sv.wikipedia.org/wiki/Valenselektron
http://www.naturvetenskap.org/hogstadiekemi/atomer/elektroner
Har atomerna 8 valenselektroner alternativt 2 om det är i K-skalet så är det yttersta skalet fullt. Det kan då inte få plats fler valenselektroner. Atomer som har fullt med valenselektroner är väldigt nöjda och glada och inte alls sugna på att reagera med andra ämnen. De atomer som är nöjda, glada och stabila redan utan att behöva göra något för att bli det kallas ädelgaser, dessa kan du läsa mer om längre ner på sidan.
Valenselektroner är som sagt de elektroner som befinner sig allra längst bort ifrån kärnan, vilket också innebär att det är dem som påverkas av minst kraft ifrån kärnan. Detta i sin tur gör att de kan reagera med andra ämnen och ge ifrån sig elektroner, eller få fler elektroner som andra ämnen gett bort. Till skillnad från oss människor som kanske inte riktigt resonerar som så att "Okej, jag har bara en cykel, då ger jag bort den!" så fungerar det lite så att ju färre valenselektroner ett ämne har, desto mer sugen är det på att ge bort dem. En detalj som kan tilläggas är väl att det inte riktigt fungerar som så att om du har en cykel och ger bort den, så kan du plötsligt ha 8 cyklar istället. Så kan det dock fungera för atomer (de har ju visserligen gett bort en elektron, och har då en elektron mindre allt som allt, men i det här fallet är cyklarna alltså valenselektroner, inte elektroner). Ger natrium bort den enda elektronen som den har i sitt yttersta skal (se tabellen ovan) så har den plötsligt 8 valenselektroner och då fullt i det yttersta skalet och känner sig genast gladare. Atomer som har fler eller färre elektroner än antalet protoner i kärnan kallas för joner. Mer om joner kan du läsa längre ner.
Källor:
http://sv.wikipedia.org/wiki/Valenselektron
http://www.naturvetenskap.org/hogstadiekemi/atomer/elektroner
Nu vet du vad en atom är för något och du vet hur atomerna är uppbyggda. Nu är det dock inte riktigt så enkelt att världen byggs upp av massor av fria atomer, utan atomerna sitter vanligtvis ihop. Atomer som sitter ihop med varandra kallas för molekyler. Atomer är små och molekyler är, inte helt oväntat, också väldigt små. Trots att det faktiskt kan vara miljontals atomer som sitter ihop med varandra så är det otroligt små (de är alltså fortfarande bra mycket mindre än tändstickor och kor, eftersom dessa faktiskt är uppbyggda av molekyler, ifall man ska fortsätta se till jämförelsen att kor och tändstickor är små).
Det kan både vara atomer av samma typ som sitter ihop och bildar en molekyl eller atomer av olika typer. Ett exempel på en molekyl som innehåller flera typer av atomer är vatten. En vattenmolekyl består av en syreatom och två väteatomer. Klorgas däremot är två atomer av klor som sitter ihop.
Källor:
http://www.naturvetenskap.org/hogstadiekemi/molekyler
http://sv.wikipedia.org/wiki/Molekyl
Det kan både vara atomer av samma typ som sitter ihop och bildar en molekyl eller atomer av olika typer. Ett exempel på en molekyl som innehåller flera typer av atomer är vatten. En vattenmolekyl består av en syreatom och två väteatomer. Klorgas däremot är två atomer av klor som sitter ihop.
Källor:
http://www.naturvetenskap.org/hogstadiekemi/molekyler
http://sv.wikipedia.org/wiki/Molekyl
Vissa ämnen består bara av en enda slags atomer, dessa ämnen kallas grundämnen. Exempel på grundämnen är svavel, klor, väte, syre, kol osv. Alla grundämnen hittar du i det periodiska systemet (mer om detta kan du läsa längre ner på sidan). Om man ska jämföra mängden grundämnen med mängden ämnen som inte bara består av en slags atomer, så finns det betydligt fler av dem andra. Nu är det dock inte så att vi bara bör utesluta alla grundämnen och mobba dem totalt, för utan dem skulle det inte finnas några andra ämnen och det vore ju ganska synd. De ämnen som inte är grundämnen är uppbyggda av diverse olika grundämnen, som sitter ihop i molekyler.
Även ett och samma grundämne kan dock se lite olika ut. Om vi tar kol som exempel. I din blyertspenna har du en blandning av grafit och kaolinlera, grafit är rent kol. Diamanter är dock också rent kol. Jämför din blyertspenna med en diamant. En klar skillnad, inte sant?
Man kan också se till ämnet syre. Sitter syreatomerna ihop två och två, blir det syrgas som är väldigt vettigt för oss att andas, utan syre så dör vi. Sitter syreatomerna däremot ihop tre och tre blir det ozon, som inte alls är lika lämplig att andas in då den är giftig. Beroende på om två eller tre syreatomer sitter ihop kan det alltså skilja på en gas som vi behöver för att överleva och en gas som är giftig att andas in.
Källor:
http://www.naturvetenskap.org/hogstadiekemi/grundamne-eller-kemisk-forening
http://sv.wikipedia.org/wiki/Ozon
Även ett och samma grundämne kan dock se lite olika ut. Om vi tar kol som exempel. I din blyertspenna har du en blandning av grafit och kaolinlera, grafit är rent kol. Diamanter är dock också rent kol. Jämför din blyertspenna med en diamant. En klar skillnad, inte sant?
Man kan också se till ämnet syre. Sitter syreatomerna ihop två och två, blir det syrgas som är väldigt vettigt för oss att andas, utan syre så dör vi. Sitter syreatomerna däremot ihop tre och tre blir det ozon, som inte alls är lika lämplig att andas in då den är giftig. Beroende på om två eller tre syreatomer sitter ihop kan det alltså skilja på en gas som vi behöver för att överleva och en gas som är giftig att andas in.
Källor:
http://www.naturvetenskap.org/hogstadiekemi/grundamne-eller-kemisk-forening
http://sv.wikipedia.org/wiki/Ozon








